CAR-T(Chimeric Antigen Receptor T)細胞療法是目前癌癥免疫治療領域備受關注的生物治療手段之一。與傳統(tǒng)的癌癥治療方式相比,CAR-T細胞療法在血液腫瘤治療中存在明顯優(yōu)勢,取得了巨大的進步。近年來,國內(nèi)CAR-T細胞療法的相關臨床試驗如雨后春筍般快速增長。根據(jù)clinicaltrials.gov網(wǎng)站的數(shù)據(jù),2017年9月,中國成為CAR-T試驗注冊數(shù)量最多的國家。截至2020年6月30日,中國注冊CAR-T試驗的數(shù)量已達357個。除此之外,已經(jīng)在ChiCTR注冊的CAR-T試驗也多達150個。
CAR-T的起源
免疫細胞療法最早起始于細胞因子技術的發(fā)展,真正意義上免疫細胞治療起始于過繼性免疫細胞療法。自1976年Morgan等人發(fā)現(xiàn)在體外可利用白介素2(IL-2)刺激T細胞大量增殖后,科學家就開始利用IL-2誘導淋巴因子激活的殺傷細胞(LAK),用于治療黑色素瘤等多種惡性腫瘤,這是早期嘗試的過繼性免疫細胞療法。過繼細胞轉移也是當時創(chuàng)造的第一個重要術語,用于描述通過輸注免疫細胞或免疫分子介導器官異體移植排斥或治療腫瘤的療法。關于這種療法在臨床上試驗成功大約是在1980年前后,這些試驗主要是在轉移性黑色素瘤患者中輸注自體腫瘤浸潤淋巴細胞(TILs),或在復發(fā)性白血病患者中輸注同種異體供體淋巴細胞。直到20世紀90年代,轉基因技術開始被廣泛用于免疫效應細胞的基因改造,其中主要用于改造T細胞、DC細胞等。這個階段出現(xiàn)了通過使用T細胞受體(TCR)或嵌合抗原受體(CAR)來重定向T細胞的特異性,增強T細胞功能的臨床試驗嘗試,從此CAR-T細胞出現(xiàn)在免疫細胞療法的舞臺上,并逐漸成為免疫細胞治療的代表。
嵌合抗原受體(CAR)
CAR,嵌合抗原受體,是經(jīng)過基因工程改造的特異性靶向受體,實際為一種融合蛋白。結構上,主要由細胞外的抗原識別部分和細胞內(nèi)信號傳導或輔助激活的結構域組成。與基因修飾的TCR-T細胞相比,CAR-T細胞可直接識別腫瘤細胞表面的抗原,而無需抗原呈遞細胞MHC分子對抗原進行加工或呈遞(圖1)。
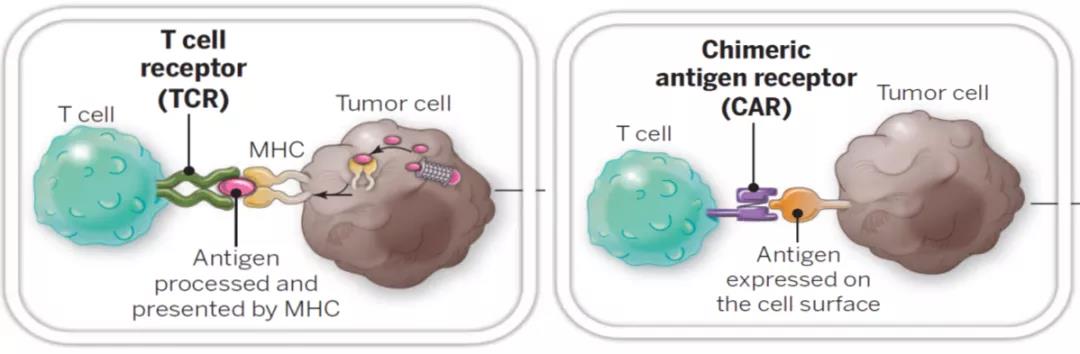
來源:Science. 2015 Apr 3;348(6230):62-8.
圖1 TCR與CAR的腫瘤抗原識別
自第一代CAR出現(xiàn)以來,即由抗CD19特異性單鏈可變片段、跨膜結構域和T細胞受體的胞內(nèi)信號傳導域(CD3ζ鏈)組成的特異性靶向嵌合受體,研究者就開始不斷對CAR進行升級迭代,提升CAR-T細胞的抗腫瘤活性。繼第一代CAR之后,第二代和第三代CAR胞內(nèi)信號轉導結構域不僅包括CD3ζ結構域,同時還涵蓋了其他信號傳導域,例如CD28,CD134,CD137(4-1BB),CD27和ICOS或組合(CD3ζ,CD28和CD134),這些結構的嵌入提升了CAR T細胞的活化、增殖和存活的能力。后續(xù)第四代CAR開始采用聯(lián)合策略,整合了表達了一些免疫分子(如,細胞因子)顯著改善了CAR-T的抗腫瘤作用。如圖2所示,通過整合IL12基因的表達系統(tǒng),嵌合有NFAT表達盒,誘導產(chǎn)生細胞因子IL12。當腫瘤抗原低表達時,CAR-T細胞無法有效識別腫瘤抗原,CAR的胞內(nèi)CD3ζ傳導信號,誘導激活轉錄因子NFAT表達,進一步誘導產(chǎn)生和釋放細胞因子IL12,激活固有免疫系統(tǒng),增加抗腫瘤活性。目前還出現(xiàn)了第五代CAR,這種CAR嵌入了IL2Rβ信號域,IL2Rβ片段可結合STAT3的YXXQ基序,誘導JAK-STAT途徑的抗原依賴性活化,促進細胞增殖,阻止終末分化,使效應細胞表現(xiàn)出更好的持久性(圖2)。
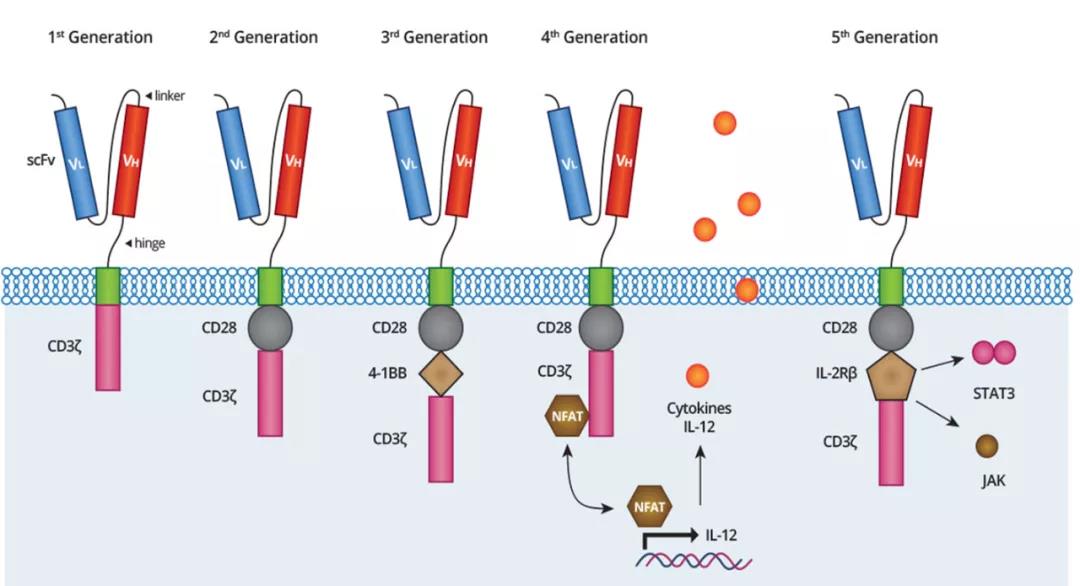
來源:Biomolecules. 2020 Feb 10;10(2):263
圖2 CAR的結構示意圖
CAR-T被輸注到患者體內(nèi)后,通過血液循環(huán)系統(tǒng)并進入到靶向的腫瘤部位,對特異性的腫瘤抗原進行識別,并通過細胞毒反應或激活免疫系統(tǒng)殺死腫瘤細胞或增強抗腫瘤活性。一方面,CD8+ CAR-T可釋放顆粒酶和穿孔素誘導腫瘤靶細胞毒性,殺死腫瘤細胞,促進腫瘤抗原釋放,誘導CAR-T細胞增殖,進一步激活免疫系統(tǒng)募集內(nèi)源性的細胞毒性T細胞,增強抗腫瘤活性;另一方面,CD4 + CAR-T細胞釋放細胞因子,激活免疫系統(tǒng)的其他成分來增強抗腫瘤活性(圖3)。同時,免疫激活后產(chǎn)生記憶性CAR-T細胞,通過免疫監(jiān)視防止腫瘤復發(fā)。
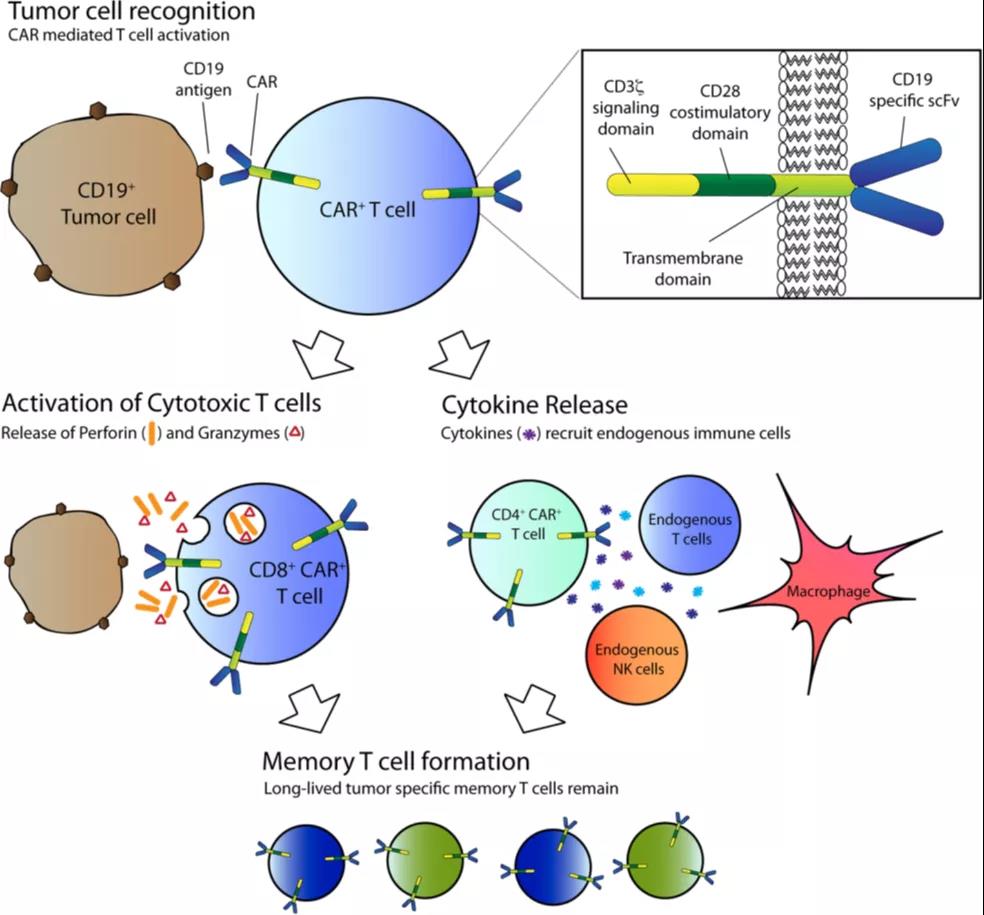
來源:Int J Hematol (2014) 99:361–371
圖3 CAR-T細胞活化和殺死靶向腫瘤細胞
CAR-T細胞治療
圖4顯示了CAR-T細胞的治療過程,主要包括:
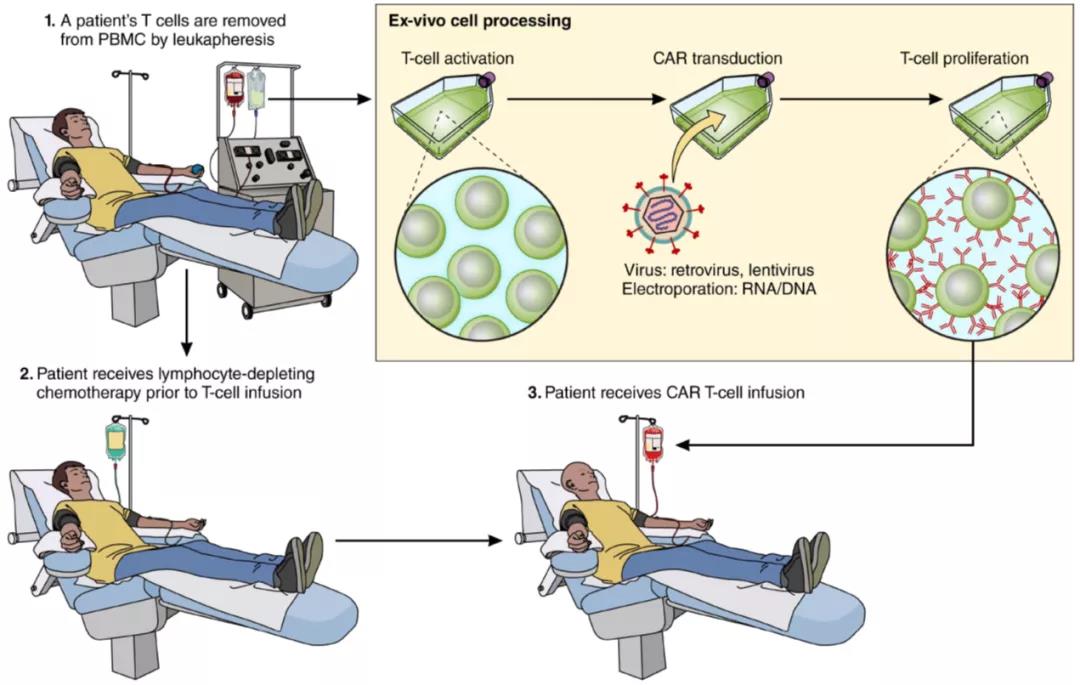
來源:Blood. 2017 Dec 14; 130(24): 2594–2602.
圖4 CAR-T細胞治療過程
目前CAR-T細胞療法還是個體化的治療方式,需要以患者的T細胞為原材料進行制備。為了避免這種個體化的治療現(xiàn)狀,研究人員也在研究通用CAR,這種CAR可用于許多不同的患者但又不會引起排斥反應;除T細胞外,其他類型的免疫細胞,例如NK細胞,巨噬細胞等,研究者在進行相關的腫瘤免疫細胞治療的嘗試。
CAR-T臨床試驗進展
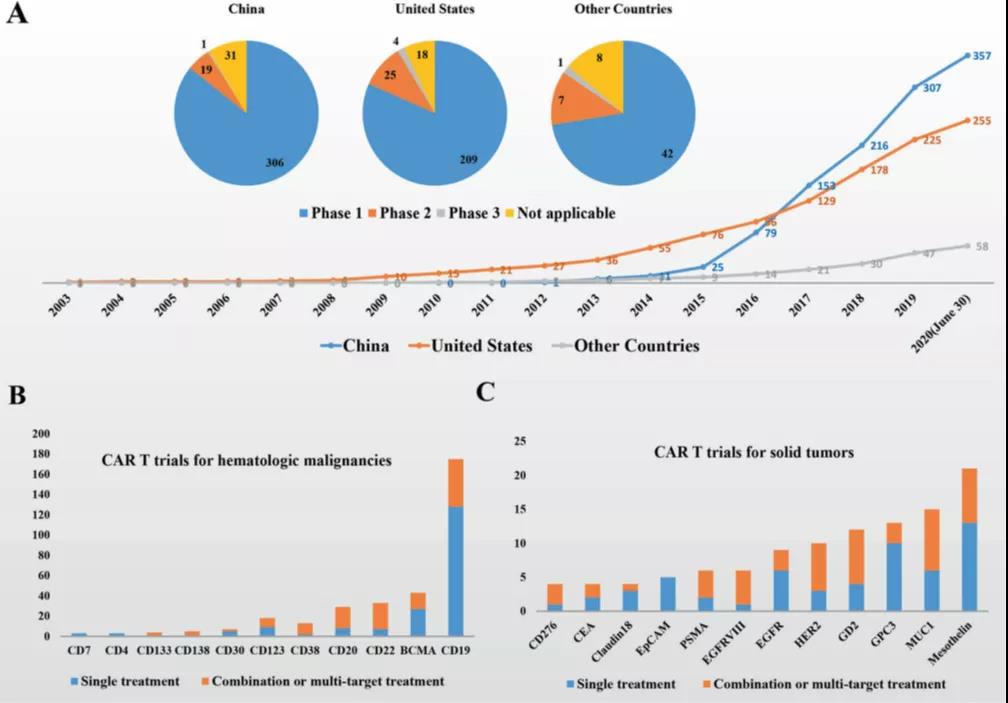
近幾年,國內(nèi)關于CAR-T細胞療法的臨床試驗如雨后春筍般快速增長。根據(jù)clinicaltrials.gov網(wǎng)站的數(shù)據(jù),2017年9月,中國成為CAR-T臨床試驗注冊數(shù)量最多的國家。截至到2020年6月30日,關于CAR-T療法的臨床試驗注冊統(tǒng)計顯示,中國境內(nèi)已注冊的臨床試驗有357項,美國256項,其他國家/地區(qū)58項(圖5A)。除此之外,已經(jīng)在ChiCTR注冊的CAR-T試驗也多達150個。
目前國內(nèi)在研的CAR-T產(chǎn)品,靶向CD19的CAR-T臨床試驗很多,共有175項(包括臺灣的2項),其中128項臨床試驗是單一靶向CD19的CAR-T療法,聯(lián)合靶向CD22的CAR-T臨床試驗有18項,聯(lián)合靶向CD20 的CAR-T臨床試驗有13項。靶向B細胞成熟抗原(BCMA)的臨床試驗位居第二,共有43項試驗,其中單一靶向BCMA有27項,另有聯(lián)合靶向CD19的有8項。除CD19和BCMA之外,還有一些其他的靶向分子用于血液系統(tǒng)惡性腫瘤的治療,如CD22,CD20和CD123等(圖5B)。
對于實體瘤的CAR-T療法,間皮素是目前主要的靶向分子,目前共有注冊的臨床試驗21項。MUC1是另一個實體瘤熱點的靶向分子,涉及共14項臨床試驗。除間皮素和MUC1外,還有其他的靶向分子如GD2,GPC3,HER2和EGFR等用于實體瘤的CAR T免疫治療(圖5C)。
根據(jù)clinicaltrials.gov網(wǎng)站的數(shù)據(jù),目前在中國的357項CAR-T臨床試驗中,臨床I期涉及306項,臨床 II期19項,III期研究1項(2020年注冊)。美國的256項CAR-T臨床試驗,I期,II期和III期研究的數(shù)量分別為209、25和4。其他國家/地區(qū)的58項CAR-T臨床試驗,I期,II期和III期研究的數(shù)量分別為42、7和1。目前,中國的大多數(shù)CAR-T臨床試驗都處于早期階段,其主要目的是驗證安全性。這可能是因為在中國,大多數(shù)試驗都是非商業(yè)性自主的研究項目,并且大部分項目缺乏被開發(fā)為藥物的潛力(圖5A)。
來源:Cell Mol Immunol. 2020 Sep 30
圖5 A. 已注冊的CAR-T臨床試驗數(shù)量和當前試驗階段的年度變化統(tǒng);
B. 當前在中國注冊的血液系統(tǒng)惡性腫瘤CAR-T臨床試驗;C. 目前在中國注冊的實體瘤CAR-T試驗
回顧CAR-T的臨床治療成果,以抗CD19為代表的CAR-T療法在血液系統(tǒng)惡性腫瘤中取得了令人矚目的成績。目前全球已有三款 CAR-T 產(chǎn)品獲批上市,分別是諾華的 Kymriah、吉利德旗下凱特制藥的 Yescarta和Tecartus。Kymriah 被批準用于治療復發(fā)難治 B 細胞前體急性淋巴性白血病 (B-ALL) 25 歲以下患者和彌漫性大 B 細胞淋巴瘤(DLBCL )成人患者;Yescarta 被批準用于治療成人復發(fā)或難治性大 B 細胞淋巴瘤患者。Tecartus 則被批準用于治療復發(fā)或者難治性的套細胞淋巴瘤(MCL)成人患者(表1)。
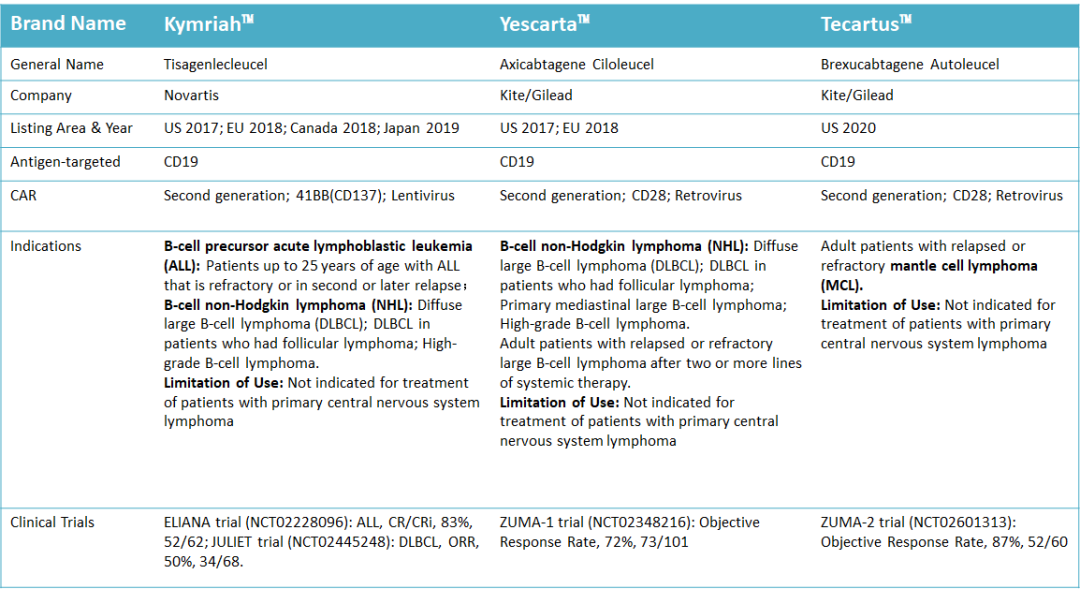
表1 全球上市的三款 CAR-T 產(chǎn)品介紹
數(shù)據(jù)來源:https://dailymed.nlm.nih.gov/dailymed
目前,國內(nèi)還未有批準上市的CAR-T產(chǎn)品,但是其中已有兩家公司在2020年提交CAR-T產(chǎn)品的上市申請。分別是復星凱特的CAR-T療法 FKC876(暫定:益基利侖賽注射液,國外商品名:Yescarta )的上市申請和藥明巨諾的 CAR-T療法 JWCAR029(暫定:瑞基侖賽注射液)是在美國 Juno 公司 JCAR017 基礎上,由藥明巨諾自主開發(fā)的靶向 CD19 的 CAR-T 療法。此外,傳奇生物 CAR-T 療法 LCAR-B38M 預計于 2021 年提交上市申請。
參考文獻:
1. Wei J, Guo Y, et al. Clinical development of CAR T cell therapy in China: 2020 update. Cell Mol Immunol. 2020 Sep 30. doi: 10.1038/s41423-020-00555-x.
2. Varadé J, Magadán S, González-Fernández á. Human immunology and immunotherapy: main achievements and challenges. Cell Mol Immunol. 2020 Sep 2:1–24. doi: 10.1038/s41423-020-00530-6.
3. Rosenberg SA, Restifo NP. Adoptive cell transfer as personalized immunotherapy for human cancer. Science. 2015 Apr 3;348(6230):62-8. doi: 10.1126/science.aaa4967.
4. Wu C, Zhang L, Brockman QR, Zhan F, Chen L. Chimeric antigen receptor T cell therapies for multiple myeloma. J Hematol Oncol. 2019 Nov 21;12(1):120. doi: 10.1186/s13045-019-0823-5.
5. Brudno JN, Kochenderfer JN. Chimeric antigen receptor T-cell therapies for lymphoma. Nat Rev Clin Oncol. 2018 Jan;15(1):31-46. doi: 10.1038/nrclinonc.2017.128.
6. Subklewe M, von Bergwelt-Baildon M, Humpe A. Chimeric Antigen Receptor T Cells: A Race to Revolutionize Cancer Therapy. Transfus Med Hemother. 2019 Feb;46(1):15-24. doi: 10.1159/000496870.
7. June CH, Sadelain M. Chimeric Antigen Receptor Therapy. N Engl J Med. 2018 Jul 5;379(1):64-73. doi: 10.1056/NEJMra1706169.
8. Davila ML, Bouhassira DC, et al. Chimeric antigen receptors for the adoptive T cell therapy of hematologic malignancies. Int J Hematol. 2014 Apr;99(4):361-71. doi: 10.1007/s12185-013-1479-5.
9. Kalaitsidou M, Kueberuwa G, et al. CAR T-cell therapy: toxicity and the relevance of preclinical models. Immunotherapy. 2015;7(5):487-97. doi: 10.2217/imt.14.123.
10. Morello A, Sadelain M, et al. Mesothelin-Targeted CARs: Driving T Cells to Solid Tumors. Cancer Discov. 2016 Feb;6(2):133-46. doi: 10.1158/2159-8290.CD-15-0583.
11. Kim DW, Cho JY. Recent Advances in Allogeneic CAR T Cells. Biomolecules. 2020 Feb 10;10(2):263. doi: 10.3390/biom10020263.
12. https://dailymed.nlm.nih.gov/dailymed; NDC Code(s): 71287-219-01, 71287-219-02; NDC Code(s): 71287-119-01, 71287-119-02; NDC Code(s): 0078-0846-19, 0078-0958-19.